Continuando o assunto das moléculas no topo do rol das que causam eutrofização (crescimento acelerado de algas uni e multicelulares) em corpos d’água, temos o nitrito (NO2–) e o nitrato (NO3-2), os quais participam do ciclo do nitrogênio.
Devido estas moléculas participarem no meio deste ciclo, faz-se importante a sua revisão e estudo aprofundado. Todos construtores e amantes de lagos devem tê-lo na “ponta da língua”.
Índice
A origem da amônia, nitrito e nitrato
O ciclo do nitrogênio (ou azoto) inicia-se com a molécula gasosa amônia (NH3) que é produzida pelo próprio metabolismo dos peixes e da maioria dos invertebrados aquáticos, pelos quais é excretada na água. Também, a NH3, pode originar-se da decomposição de resíduos orgânicos (microalgas e bactérias mortas, fezes, sobras de ração, carapaças, muco e adubos orgânicos) promovido através das bactérias presentes na água e, também, pelo uso de fertilizantes nitrogenados contendo NH3, ureia e/ou NO3-2 como os utilizados em pisciculturas (veja a Figura 1).

Figura 1. Principais fontes de amônia, e consequentemente de nitrito e nitrato, nos tanques de cultivo de peixes e camarões. Fonte: Panorama da Aquicultura, vol. 27, n.164.
Na sequência, a NH3 conjuga-se a um próton hidrogênio (H+) transformando-se em íon amônio / amoníaco (NH4+), conhecido ainda como amônia não-tóxica. O NH4+, por sua vez, é convertido em NO2– através da reação de nitrosação abaixo, realizada pelas bactérias aeróbias do gênero Nitrosomonas sp e Nitrosococcus sp:
(amônio) (nitrito)
NH4+ + 1 ½ O2+ → 2H+ + NO2– + H2O + energia
Continuando o ciclo, o Nitrito (NO2–) é convertido em Nitrato (NO3-2) através da reação de nitração efetuada pelas bactérias do gênero Nitrobacter sp, como na reação abaixo:
(nitrito) (nitrato)
NO2– + ½ O2 → NO3-2
O gás nitrogênio para finalizar o ciclo
Apenas para terminar o ciclo, o NO3-2 é convertido em nitrogênio (N2) gasoso através de bactérias anaeróbias, como as do gênero Clostridium sp. Este processo é denominado desnitrificação e libera o N2(g) de volta para a atmosfera.
Nitrito e nitrato na eutrofização do lago
Retornando ao assunto do nitrito e nitrato e sua atuação na eutrofização dos corpos d’água, como vimos com o fosfato anteriormente, o nitrogênio de suas moléculas pode ser utilizado para o desenvolvimento das algas e macrófitas (plantas aquáticas como a alface d’água, a vitória régia, a ninfeia, etc), principalmente do nitrato.
Dentro destes organismos, assim como em qualquer outro ser vivo, o nitrogênio participará de todas as proteínas, já que é responsável por conectar um aminoácido ao outro numa ligação chamada de peptídica (ver Figura 2). Além disso, o nitrogênio também fará parte do material genético (bases nitrogenadas do DNA e do RNA) e da molécula energética, o ATP (adenosina tri-fosfato – ver Figura 3).
Boom de algas
Enfim, uma grande concentração de nitrogênio na água, seja no formato de nitrito e nitrato ou, até mesmo, de amônia ou amônio, pode ser considerado como “alimento” para o grande e rápido desenvolvimento das algas ocasionando visivelmente um “boom” de algas dentro de um corpo d´água.
Este “boom” de algas tem grande prejuízo para os peixes, pois consomem o oxigênio da água, principalmente à noite (fase escura da fotosíntese), e podem matá-los por sufocamento (hipóxia – baixa concentração de oxigênio na água). Temos também a redução da transparência da água, presença de odor, substâncias tóxicas que podem ser eliminadas por algumas espécies de algas, entre outros.
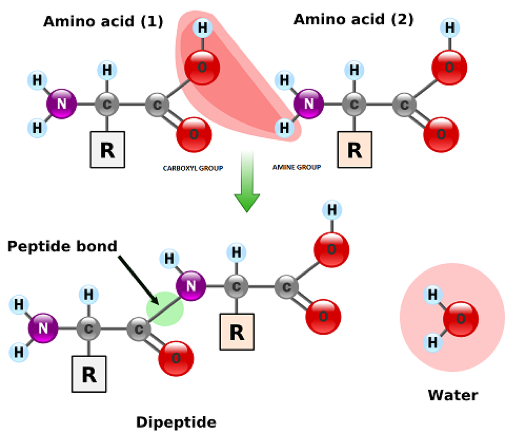
Figura 2. Reação de ligação de dois aminoácidos (Amino acid 1 + Amino acid 2) para a formação de um dipeptídeo, chamada de ligação peptídica (peptide bond). Fonte: http://mundodabioquimica.blogspot.com.br/2015/01/ligacao-peptidica.html

Figura 3. Estrutura química da molécula de ATP (adenosina Tri-Fosfato), destacando a presença do nitrogênio. Fonte: https://cen.acs.org/articles/95/i21/New-role-cells-suggested-ATP.html
Concentração máxima de nitrito e nitrato
Outro aspecto importante são os efeitos deletérios do nitrito e nitrato para os peixes. Segundo um resumo publicado na Panorama da AQÜICULTURA (nov/dez 2017), a concentração letal de 50% dos animais em 4 dias, que é chamada de CL50 – 96h, para estas moléculas é de 66,6 mg/L e 467mg/L, respectivamente, em carpa comum.
No entanto, recomenda-se uma porcentagem de 10% desse valor como um limite máximo seguro para a espécie, devendo ficar abaixo de 6,6mg/L e 46,7mg/L de nitrito e nitrato, respectivamente. Uma vez que esta concentração está elevada na água, tais moléculas são absorvidas para o corpo dos peixes pelas brânquias.
O nitrito e a oxigenação do sangue nos peixes
Na corrente sanguínea, o nitrito oxida o íon ferro (do estado Fe+2 para Fe+3) contido na molécula de hemoglobina das células vermelhas, as hemácias. Estas células são responsáveis por transportar o oxigênio para todo o corpo do animal e, na presença de nitrito, elas perdem esta capacidade causando mortalidade por “sufocamento”, ou melhor, hipoxemia (baixas concentração de oxigênio no sangue) mesmo os animais estando em águas com altas concentrações de oxigênio.
Visivelmente, a coloração do sangue deixa de ser um vermelho vivo para ficar um sangue amarronzado, como chocolate, característica de sangue com pouco oxigênio e que pode ser visto abrindo-se os opérculos deles.
Essa baixa concentração de oxigênio no sangue é muito ruim para os peixes, pois promoverá um baixo metabolismo aeróbico do animal e, consequentemente, uma redução na taxa de crescimento e baixa resistência dos peixes às doenças. Os efeitos são “desastrosos” para a piscicultura.
A osmorregulação
Há nas brânquias dos peixes, células com trocadores iônicos que são responsáveis por enviar íons da água para o sangue em troca da excreção de íons do sangue para água, o que é denominado em fisiologia de osmorregulação.
Uma destas células é denominada célula cloreto, a qual envia para dentro da célula (consequentemente para o sangue) íons cloreto (Cl–) em troca de íons bicarbonato (HCO3–) (veja figura 4).
Quando há elevado nível de nitrito (NO2–) na água, ele compete pelo mesmo trocador iônico com o Cl– e pode entrar na célula e causar os efeitos acima citados, o que explica o porquê do nitrito ser muito mais tóxico que o nitrato.
Assim, uma das formas de se evitar essa “competição” do nitroto com o Cl–, e até mesmo resolver essa situação que pode ocorrer principalmente em pisciculturas, é aumentar a quantidade de Cl– na água, através de sal não iodado. Isto promoverá uma redução na toxidez ocasionada pelo nitrito. A quantidade de sal recomendada a ser aplicada é de 6 a 10 unidades de Cl- para cada unidade de NO2– ou, até mesmo, numa proporção de 20:1 segundo a matéria da Panorama da AQUICULTURA (vol. 103:17, p. 14-23).

Figura 4. Célula cloreto α de teleósteo de água doce mostrando trocas iônicas e, no caso, o trocador iônico Cl– / HCO3–Fonte: http://www.uel.br/laboratorios/lefa/aulas/Aulas2e3osmorregulacao2011.pdf

Thiago de Campos Belão é Biólogo, mestre e doutor em Ciências Fisiológicas pela UFSCar. Especializou-se em fisiologia animal com enfase em peixes tropicais e, principalmente, nas áreas de comportamento animal, metabolismo, toxicologia e nos sistemas cardiovascular, respiratório e nervoso central e periférico.


Boa tarde, gostaria de saber se somente com a análise de nitrato é possível avaliar a saúde do lago ou é necessário nitrato e amônia?
Qual tipo de método e/ou equipamentos vocês costumam usar para medir pH, OD, amônia e nitrato?
Fábio, o correto é avaliar os três parâmetros. Existem kits de teste no mercado e você encontra em qualquer loja de aquário.
Gostaria de saber como faço para abaixar o nível do nitrito. Está alto e um peixe já morreu com a coloração marrom na área da cabeça
Oi José, boa tarde. O que baixa o nitrito é a filtragem biológica. Precisa rever a sua filtragem. Vou te enviar um e-mail. Abraços.
existe nitrito alto com amonia zerada ?
Eduardo, precisamos entender melhor o contexto. Nos envie um e-mail para atendimento@cubos.com.br
Bom dia, gostaria de saber porque determinar o nitrogênio amoniacal, o nitrogênio nitrito, o nitrogênio nitrato e o nitrogênio total na análise do solo sabendo que o nitrogênio se desloca ou se perde com facilidade. E que no manual de adubação do estado da Bahia não existe recomendação para nitrogênio em cima do resultado da análise de solo e sim de acordo com a idade da planta.
Olá Hércules. O nitrogênio que estamos tratando no artigo é o dissolvido na água e não o presente no solo. Nossa área é de tratamento de peixes. Att.
Excelente matéria. Parabéns e obrigado. Mas aproveito para perguntar, como se estima a quantidade de plantas filtrantes necessárias para um determinado volume dagua. Há algum texto sobre o assunto?
Oi Miguel, tudo bem? Se for um lago só com filtragem de plantas, o ideal é ter pelo menos 1/3 da área do lago na filtragem de plantas. Se o lago já tiver filtragem biológica, as plantas irão auxiliar, quanto mais melhor. Mas tem que saber escolher as plantas certas, o ideal são as de crescimento rápido.